Projekt specustawy regulującej dostępność środków antykoncepcyjnych w Polsce śledzę od przeszło roku, niemal od pierwszych doniesień o tym, że Ministerstwo Zdrowia pracuje nad takimi zmianami. Od roku też, jako członek partii Razem, jestem zaangażowany w informowanie o skandalicznej treści, uzasadnieniu i skutkach tej ustawy.
Minister Konstanty Radziwiłł w wielu publicznych wypowiedziach podkreśla, że zmiana kategorii dostępności „pigułki po” jest konieczna z uwagi na doniesienia, jakoby był to lek masowo nadużywany. Szczególną jego troskę wzbudza nadużywanie przez osoby nieletnie, na sercu leży ministrowi też bezpieczeństwo kobiet. Tak przynajmniej mówi.
Podczas obrad sejmowej komisji zdrowia, w których uczestniczyłem, przedstawiciele Ministerstwa Zdrowia nie potrafili przekonująco obronić uzasadnienia wprowadzenia proponowanych zmian. W trakcie dyskusji na posiedzeniu komisji ministerstwo stało na stanowisku, że ograniczenie dostępności antykoncepcji awaryjnej jest uzasadnione bliżej nieokreślonymi „doniesieniami” o masowym nadużywaniu tabletek „dzień po”. Ponadto w trakcie drugiego posiedzenia wiceminister Zbigniew Król przyznał otwarcie, że ministerstwo nie dysponuje badaniami klinicznymi, które popierałyby tezy zapisane w uzasadnieniu projektu. Uzasadnienie projektu jest zatem merytorycznie bardzo wątpliwe – opieranie się w medycynie na lękach płynących z anegdotycznych dowodów po prostu nie uchodzi. Skoro więc uzasadnienie medyczne nie istnieje, to jakie jest realne podłoże tej ustawy? Tego też na komisji się nie dowiedzieliśmy. W zamian ministrowie, posłanki i posłowie prawicy powtarzali jak mantrę: „Antykoncepcja doustna w całości i zawsze była na receptę, więc na receptę być musi nadal. To silnie działające leki.” Dziwna to tradycja, ale najwyraźniej warto ją utrwalać z uporem godnym lepszej sprawy.
Opieranie się w medycynie na lękach płynących z anegdotycznych dowodów po prostu nie uchodzi.
Słuchając wypowiedzi polityków o projekcie ustawy, trudno nie odnieść wrażenia, że ich wiedza na temat ustalania kategorii dostępności leków jest bardzo powierzchowna. Wiceminister Król, pytany podczas obrad komisji zdrowia przez przewodniczącego Bartosza Arłukowicza o odpowiednie przepisy będące podstawą dla jego argumentacji, nie potrafił odnaleźć w pamięci nic ponad to, że kategoria dostępności jest ujęta w charakterystyce produktu leczniczego.
Dla czytelników i pana ministra telegraficzny skrót praw dotyczących ustalania kategorii dostępności produktów leczniczych:
Na poziomie prawa unijnego tryb ustalania kategorii dostępności leków opisuje dyrektywa 2001/83/EC, z którą krajowa ustawa Prawo Farmaceutyczne i towarzyszące mu rozporządzenie MZ (Dz.U. 2008 nr 206 poz. 1292) są jednobrzmiące. Kategorię dostępności zarówno na poziomie unijnym jak i krajowym ustala się przy rejestracji produktu leczniczego lub zmienia po owej rejestracji na wniosek producenta, przy czym Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych (w skrócie, choć co ta za skrót, URPLWMiPB) oraz Europejska Agencja ds. Leków (EMA) ustalają na podstawie badań klinicznych dostarczonych wraz z wnioskiem, czy produkt leczniczy wyczerpuje którąś z ujętych przepisami definicji produktu dostępnego na receptę.
Jednym z wątków wielokrotnie podnoszonych przez producenta i gości komisji zdrowia podczas jej prac jest niezgodność prawa krajowego i unijnego. Autorzy projektu wprawdzie powołują się na zapisy wspomnianej wyżej dyrektywy 2001/83/EC przewidujące krajowe wyjątki w regulacji dostępności środków antykoncepcyjnych i poronnych, jednak zupełnie niezrozumiałe jest nieuzasadnione medycznie wprowadzanie dodatkowego, nieprzewidzianego tą dyrektywą trybu ustalania kategorii dostępności.
Kolejnym problemem jest nadanie nowym rozwiązaniom rangi ustawy: uchylenie przepisów wymagać będzie przejścia całej ścieżki legislacyjnej, a w rezultacie nawet posiadania większości 2/3 głosów w sejmie (w wypadku gdyby sejm miał odrzucać weto prezydenta w tej kwestii).
Resort najwyraźniej nie zdaje sobie również sprawy z faktu, że treść proponowanych przepisów jest niezgodna z uzasadnieniem ich uchwalenia.
W uzasadnieniu projektu mowa o zmianie kategorii dostępności środków z grupy ATC G03A, czyli hormonalne środki antykoncepcyjne do stosowania wewnętrznego. W projekcie mamy już zapis dotyczący wszystkich środków do stosowania w antykoncepcji. Skutkiem takiej ustawy będzie również zmiana kategorii dostępności produktów leczniczych do stosowania miejscowego (żele i globulki z nonoxynolem). Również tych jeszcze nie wynalezionych.
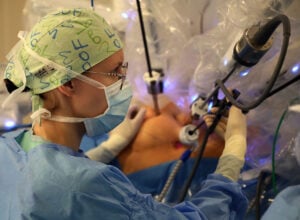
Bardzo pouczająca jest też lektura raportu EMA z przebiegu procedury zmiany kategorii dostępności EllaOne – wśród badań przedstawionych przez producenta, by dowieść, że lek nie wyczerpuje definicji leku na receptę w rozumieniu dyrektywy 2001/83/EC, aż dwa dotyczące nieprawidłowego stosowania prowadzone były m.in. w Polsce.
W ocenie EMA producent EllaOne dowiódł, że lek może być bezpiecznie i samodzielnie stosowany przez pacjentki oraz że jego stosowanie nie jest związane z wysokim ryzykiem niepożądanych zdarzeń.
Nasze Ministerstwo Zdrowia niestety woli przyjąć bujdy ultrakonserwatywnych środowisk za uzasadnienie swojego skandalicznego projektu. Jako farmaceucie jest mi po prostu za ministerstwo wstyd.
Jerzy Przystajko – aptekarz z Opola, kierownik apteki w małym miasteczku na Opolszczyźnie. Członek Rady Krajowej Partii Razem.
We wtorek 9 maja o 17.00 pod sejmem odbędzie się pikieta Prawa Kobiet Bez Recepty.

 Wspieraj
Wspieraj 

 Wspieraj
Wspieraj  Wydawnictwo
Wydawnictwo 
 Przekaż
Przekaż 

![Piotr Wójcik "Trumponomika [o ekonomii Donalda Trumpa]"](https://krytykapolityczna.pl/wp-content/uploads/2022/12/plomienie_trumponomika-okladka-171x267.jpg)

![Utracony kompas [o europejskiej lewicy]](https://krytykapolityczna.pl/wp-content/uploads/2026/03/plomienie_utracony_kompas-171x267.jpg)











Komentarze
Krytyka potrzebuje Twojego głosu. Dołącz do dyskusji. Komentarze mogą być moderowane.